Kimyasal Tepkimeler Özet 5
İNDİR
KİMYASAL TEPKİMELER
Kimyasal Tepkimeler Özet 5
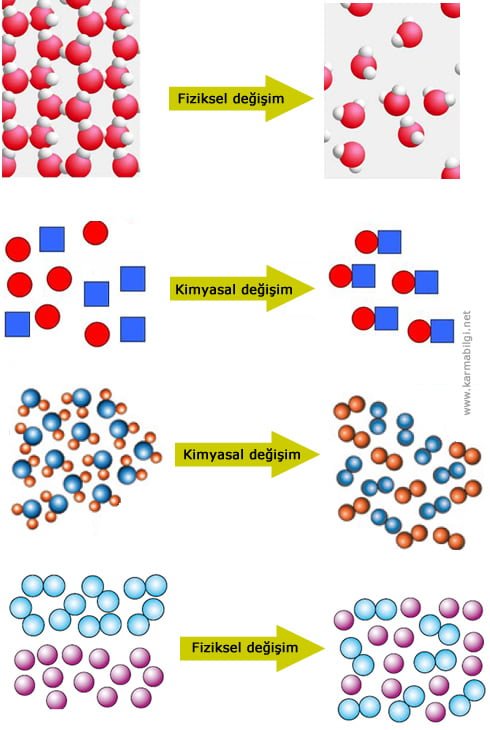
Günlük yaşamımızda birçok değişim gözleriz. Bunlardan bazılarının sadece görünümü değişirken, bazılarının ise yapısı değişir.
Örneğin buz eriyince su olur. Suyu yapısında bir değişme olmaz. Yumurtanın pişmesinde ise yumurtanın yapısı değişir. Yeni bir madde oluşur. 6. Sınıf fiziksel ve kimyasal değişme konusundan hatırlamış olmamız gerekir.
Maddenin içyapısında meydana gelen ve yeni bir madde oluşumuna kimyasal tepkime (kimyasal değişim) denir.
- Kimyasal tepkimelerde genellikle ısı, ışık, gaz çıkışı, renk değişimi ve çökelek oluşumu meydana gelir.
- Yanma, kokuşma, paslanma, yaprağın sararması, canlıların büyümesi, sindirim, solunum, fotosentez gibi olaylar kimyasal tepkime sonucunda oluşur.
Fiziksel değişmelerde maddenin içyapısı değişmez, maddenin tanecikleri arasındaki boşluk ve maddenin dış görünüşü değişir. Yeni bir madde meydana gelmez.
- Örnek: Suyun donması, kâğıdın yırtılması, camın kırılması, şekerin suda çözünmesi…
Kimyasal değişim nasıl olur? Bu sorunun cevabını şu şekilde vermeye çalışalım.

Kimyasal değişmelerde yeni maddeler oluştuğuna göre maddeyi oluşturan taneciğin yapısı değişmiştir. Yani atomlar arasındaki bağlar kopar ve farklı bağlar oluşur.




Su (H2O) oluşurken hidrojen (H2) gazındaki H-H bağı ve oksijen (O2) gazındaki O-O bağı kopar ve yeni H-O bağları oluşur.
Kimyasal Tepkimeler Özet 5
KİMYASAL TEPKİMELERDE KÜTLENİN KORUNUMU
Kimyasal tepkimelerde atomlar arası bağlar kopar ve yeni bağlar oluşur. Bu gerçekleşme sırasında atomların türleri ve sayıları değişmez. Bu nedenle tepkime öncesi ve sonrası kütle değişmez yani korunur.
Kimyasal tepkimelerde;
1. Kütle korunur.
2. Toplam proton ve nötron sayısı korunur.
3. Toplam elektron sayısı korunur.
4. Atom sayısı ve çeşidi korunur.
5. Toplam yük korunur.
Bir kimyasal tepkimede girenlerin kütleleri toplamı ürünlerin kütleri toplamına eşittir.
A+B → C+D
mA + mB = mC + mD dir.
m: kütle
Örnek: 6 g karbon 16 gram oksijen il yanınca kaç gram karbondioksit oluşur?
Karbon + Oksijen Karbondioksit
6 g 16 g ?
6 + 16 = ?
? = 22 g karbondioksit gazı oluşur
KİMYASAL DENKLEMLERİN DENKLEŞTİRİLMESİ
Kimyasal tepkimelerde atom türlerinin, atom sayılarının ve kütlenin eşit olması için tepkime denkleminin girenler ve ürünlerdeki element ve bileşik sembollerinin önüne uygun katsayı yazılır. Bu katsayılar element ya da bileşikler ile çarpım durumundadır.
Kimyasal tepkimeler denkleştirilirken kural;
1- Denklem denkleştirilirken genellikle yapısında en fazla atom bulunan taneciğin önüne 1 katsayısı yazılır.
2- H ve O atomları dışındaki elementler öncelikle sayma yöntemi ile eşitlenir ve bu iki atom en sona bırakılır.
3- Bir tepkime genellikle en küçük tam sayılar kullanarak denkleştirilir.
H2 + Cl2 → HCl tepkimesini denkleştirelim. Bütün element ve bileşiklerdeki atom sayısı eşit durumda, O halde herhangi birisinin katsayısını bir alalım. Girenler tarafında hangi atomdan kaç tane var ise ürünler tarafında da aynı atomdan o kadar bulunmalıdır. H atomu girenler tarafında 2 tane o zaman ürünler tarafında da 2 tane olmalıdır. Ürünler tarafında H 1 tane olduğunda katsayısına 2 yazılmalıdır.
H2 + Cl2 → 2HCl Girenler tarafında Cl 2 tane ürünler tarafında 2×1=2 tane oldu, o halde denklemimiz denkleşmiş oldu.
SORU: Al(OH)3 + H2SO4 → Al2(SO4)3 + H2O Denklemini en küçük sayılarla denkleştiriniz.
Çözüm: Atom sayısı en fazla olan Al2(SO4)3 bileşiği olduğundan katsayısını 1 yazalım.
Al(OH)3 + H2SO4 →1Al2(SO4)3 + H2O
Katsayısını 1 aldığımız bileşikte ilk sırada Al atomu var. 2×1=2 tane o halde girenler tarafında da iki tane olacaktır. Al(OH)3 te 1 tane olduğundan katsayısını 2 yazmalıyız.
2Al(OH)3 + H2SO4 → 1Al2(SO4)3 + H2O
Al atomunu denkleştirdikten sora S atomuna sıra geldi. 1x3x1= 3 tane bulunmaktadır. Girenler tarafında da 3 tane olmalıdır. H2SO4 bileşiğinde 1 tane S atomu bulunduğunda katsayısına 3 yazmalıyız.
2Al(OH)3 + 3H2SO4 → 1Al2(SO4)3 + H2O
Girenler tarafında katsayı yazacağımız başka bileşik ya da element kalmadığında girenler tarafındaki atomların sayısına bir bakalım. Al ve S atomlarının sayısını eşitledik. H ve O atomlarının sayısına bakalım.
2Al(OH)3 bileşiğinde H sayısı 2 x 1 x3 = 6 tane H
3H2SO4 bileşiğinde H sayısı 3 x2 = 6 tane H
6 +6 = 12 Tane H girenler tarafında o halde ürünler tarafında da 12 tane H olacaktır.
Ürünler tarafında sadece H2O da H atomu var. H2O bileşiğinde 2 tane H atomu var. 12 tane olabilmesi için 12/2=6 dan katsayısı 6 olmalıdır.
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
- NO + O2 → NO2
- H2 + O2 →H2O
- H2 + Cl2 →HCl
- Mg + O2→ MgO
- Na + Cl2→ NaCl
- Ag + O2 →Ag2O
- Fe + Cl2→ FeCl3
- Br2 + KI→ KBr + I2
- CH4 + O2 → CO2 + H2O
- C3H8 + O2 → CO2 + H2O
- C5H12 + O2 → CO2 + H2O
- C7H16 + O2→ CO2 + H2O
- C9H20 + O2 → CO2 + H2O
- C2H4 + O2 → CO2 + H2O
- KClO3 →KCl + O2
- Ca + H2SO4→ Ca SO4 + H2
- Ca(OH)2 + HCl→ CaCl2 + H2O
- NaOH + H2SO4→ NaSO4 + H2O
- NaOH + H3PO4 → Na3PO4 + H2O
- HCl + Zn →ZnCl2 + H2
- H2SO4 + Cu→ CuSO4 + H2
Kimyasal Tepkimeler Özet 5